Дорогие специалисты ультразвуковой диагностики!
Ожирение становится эпидемией, и УЗИ печени, которое раньше было узкой специализацией, превратилось в неотъемлемую составляющую почти каждого ультразвукового исследования брюшной полости, проводимого пациентам в возрасте от 10–12 лет и до глубокой старости.
Я начну с жировой инфильтрации (стеатоз). Это самая распространенная причина воспаления** печени, ведущая к фиброзу, который впоследствии может прогрессировать в цирроз печени. Распознавание жировой болезни печени и фиброза — основная задача серошкальной УЗ диагностики.
Такие исследования сильно зависят от настроек оборудования. С 1980-х годов технический прогресс в этой области или очень медленный или вообще отсутствует, а движимое «отчаянием» ультразвуковое сообщество в последнее время очень заинтересовалось различными формами эластографии.
Я считаю, что во всех последних сканерах заводские предварительные настройки для визуализации печени позволяют работать только с крайними формами вышеуказанных состояний, поэтому, используя эти настройки, вы полностью упускаете возможности ранней диагностики, которые открывает ультразвук.
Меня часто удивляют научные публикации, касающиеся исследования жировой болезни печени с помощью различных форм МРТ. Обычно в них присутствует некое предложение, в котором говорится, что ультразвуковое исследование «может применяться, однако не позволяет проводить количественную оценку», далее в завершение сложного анализа приводятся несколько качественных категорий, подобных традиционной визуальной градации, типичной для радиологии и патанатомии.
Кажется, мы все хотим иметь простые количественные показатели, которые можно применять к сложным аспектам нашей работы, однако часто это невозможно или неэффективно. МРТ, конечно, отличный инструмент, однако он не позволяет быстро и дешево проводить амбулаторный скрининг, чем ежедневно занимаются специалисты ультразвуковой диагностики.
Я покажу вам, как можно улучшать ультразвуковые изображения независимо от используемой УЗ системы и получать множество дополнительной информации с помощью старого компьютера, который просто стоит у вас в кабинете (или дома).
Печень становится «жирной», когда триглицериды накапливаются в цитоплазме гепатоцитов, сначала в форме крошечных везикул, некоторые из которых впоследствии объединяются в более крупные глобулы, которые могут вытеснять ядра или другим образом деформировать клетку. Все эти везикулы, конечно, намного меньше самой короткой длины волны, применяемой в УЗ диагностике.
Ультразвуковые находки обусловлены явлениями по типу преломления и «расфокусировки»УЗ сигнала/луча, а также рассеяния. Обычно мы видим печень нормального размера и формы с нормальной сосудистой структурой — повышенной эхогенности (т.е. с жировой инфильтрацией) без значимого затухания УЗ сигнала.
На изображении паренхимы имеются множество мелких «спеклов»*** и повышенный шум. Обычно нет значиго затухания УЗ сигала, изображение печени визуализируется до почки, печень намного более эхогенная, чем почечная паренхима. При не слишком высоком усилении можно также заметить «дребезжание» сигналов дистальнее печеночных вен.
При наличии отрицательного градиента между свойствами крови в сосуде и окружающих сосуд клеток печени с жировой инфильтрацией круглое поперечное сечение сосуда действует как собирательная линза, которая фокусирует луч и способствует увеличению обратного рассеяния. Это может быть трудно заметить, но если вы все же это видите, а в остальном печень выглядит нормально, возможно следует отметить необходимость повторного исследования через некоторое время и подсказать направляющему врачу, что неплохо бы назначить кое-какие анализы (например, на триглицериды в сыворотке).
Между ожирением и жировой инфильтрацией печени существует явная связь. Когда к вам приходит пациент весом 135 кг, вы ожидаете увидеть жировой гепатоз, однако это случается не всегда. Иногда можно испытать шок, увидев то, что кажется жировой инфильтрацией печени, у человека с нормальным индексом массы тела (ИМТ) и отсутствием в анамнезе чрезмерного или продолжительного потребления алкоголя, других состояний или приема препаратов, которые могут провоцировать стеатоз печени.
Принято считать, что жировая дистрофия печени— это часть метаболического синдрома, который проявляется клинически после десяти или более лет постоянного субклинического нарушения. Я рассматриваю жировую дистрофию печени как причину или стимулирующий фактор метаболического синдрома, поскольку это первое, что обнаруживается с помощью ультразвука.
Большинство моих пациентов — это женщины, направленные гинекологами, некоторые из них по каким-то причинам предварительно сдают рутинные анализы на холестерин, триглицериды или гемоглобин A1C. Кстати, жировая дистрофия печени чаще встречается у мужчин, чем у женщин.
Ранние стадии стеатогепатоза обратимы. Если я обнаруживаю жировую дистрофию печени у полных пациентов, я рассказываю им, что люди, у которых в печени откладывается или накапливается жир, подвержены риску гипертонии и диабета, а также осложнений, связанных с этими состояниями. Как правило, они начинают серьезнее, чем раньше подходить к похудению и упражнениям.
Я подозреваю, что в будущем лечение жировой дистрофии печени (как с другими признаками метаболического синдрома, так и без них) будет включать медикаментозное лечение статином, который ограничивает воспалительный компонент, ускоряющий клиническое ухудшение у таких пациентов. В последнее время также наблюдается интерес к использованию в качестве профилактического средства куркумина, активного ингредиента специи кукурмы, однако необходимо еще решить проблему биологической доступности и дозировки.
Точное определение жировой дистрофии печени (жир составляет 5,5% или более веса печени) требуется для научной работы. Что касается принятия клинических решений, если внутрипеченочный жир обнаруживается с помощью ультразвука, это достаточное основание для принятия профилактических мер. Жировая болезнь печени в настоящее время встречается у 15% населения Китая и 30% населения США.
По прогнозам, неалкогольная жировая дистрофия печени станет заболеванием №1 в мире менее чем через десять лет. Стеатогепатоз прогрессирует в фиброз или цирроз у сравнительно небольшого процента пациентов, однако нагрузка, которую метаболический синдром и его осложнения создадут на любую систему здравоохранения, будет очень большой. С помощью рутинных ультразвуковых исследований, которые включают исследование печени, можно обнаружить наличие данного состояния на стадии, когда оно поддается лечению.
Пациенты, которые приходят ко мне по направлениям, в основном белые и латиноамериканцы (в основном мексиканцы), а также немного афроамериканцев и азиатов. Это преимущественно, но не исключительно женщины, в основном взрослые, а не дети. Если говорить о жировой дистрофии печени, то она непропорционально чаще встречается у латиноамериканцев (женщин и мужчин), чем у других этнических групп. Такое же наблюдение было сделано в нескольких серьезных исследованиях с большими группами пациентов и точной характеризацией жировой дистрофии печени.
Наивно предполагать, что причиной жировой болезни печени является только питание, это неверно. Очевидно, что, когда заболеваемость существенно варьируется в зависимости от этнической группы, должен присутствовать генетический фактор (или, как обычно, факторы). В последние годы было получено много информации о генетике жировой дистрофии печени. Она сложная. Согласно подтвержденному открытию, один нуклеотидный полиморфизм (ОНП) гена, который отвечает за окисление жирных кислот, особенно часто встречается у латиноамериканцев.
Посмотрите на изображение ниже. Есть еще одно практическое соображение, связанное с визуализацией стеатогепатоза. Мы привыкли рассматривать жировую болезнь печени как «диффузное» заболевание, которое равномерно поражает печень. Первые несколько раз, когда вы видите округлый гипоэхогенный «узел» в жировой печени, вы предполагаете, что это метастатический очаг, даже если это по совокупности признаков не очень похоже на метастаз.
Я помню, что проводил несколько биопсий таких «узлов» под ультразвуковым контролем еще в 1980-х годах. Результатом всегда была «нормальная печень». Конечно, мы переживали, что биопсия могла «промахнуться» мимо образования, пока не поняли, что на самом деле это были островки нормальной печени, которые еще не были подвержены или каким-то образом были устойчивы к накоплению жира. На следующем изображении участок на периферии не вовлечен в процесс жировой дистрофии.
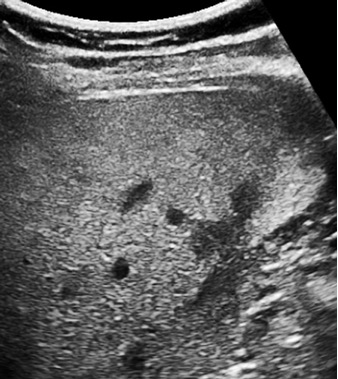
Умеренная жировая дистрофия печени 42-летней женщины с более выраженным участком в задней части правой доли печени, прилегающим к неподверженным жировым изменениям периферийным участкам.
С 1990-х, во многом благодаря КТ, стало известно, что жировая дистрофия печениможет состоять из различных зон жировой инфильтрации и нормальной ткани. Я однажды видел правую долю, которая выглядела как знак инь-янь с гиперэхогенной верхней частью и криволинейной границей над нормальой нижней частью. Вот почему я это вспомнил: если причина в ОНП, вы увидите диффузное распространение и поражение всех клеток и нечто абсолютно другое в случае генетического мозаицизма.
Это явление хорошо известно в дерматологии: системные заболевания на коже проявляются «пятнами» или участками вдоль дерматом. Сыпь появляется в клетках с «плохим» ОНП. Возникает более простой вопрос: какая на самом деле инфильтрация — диффузная или зональная?
Это важно, когда мы пытаемся взять на анализ небольшую часть печени с помощью биопсии или используем область интереса, например при эластографии. Какими должны быть объем и частота выборки? Вероятно, на этот вопрос можно ответить, если речь идет о прогрессирующей опухоли. В случае зональной жировой инфильтрации или фиброза могут возникнуть трудности.
Я не буду много рассказывать о второй стадии разрушения печени — воспалении. Воспаление, по сути, не оказывает существенного влияния на ультразвуковые изображения. Я предполагаю, что к тому времени, когда мы уже обоснованно уверены в наличии жировой инфильтрации, небольшой воспалительный компонент уже присутствует, а любые изменения в мелких сосудах намного меньше тех, которые могут быть обнаружены с помощью допплера.
Между прочим, действительно чувствительный доплер был бы волшебным инструментом, ведь адипоциты при ожирении выделяют вазоактивные факторы, которые ограничивают кровоток, вызывая гипоксию участка, и способствуют выделению воспалительных факторов, что ведет к гипертрофии адипоцитов. Это противоположно тому, что мы ожидаем при воспалении в любой другой части организма.
Самое главное, что я усвоил из молекулярной биологии и геномной медицины, это то, что физиологические и патофизиологические процессы невероятно сложны. Жировые клетки такие же сложные, как и любые другие клетки. Если я знаю, что при ожирении адипоциты выделяют в кровь повышенный уровень лептина, который способствует гипертрофии миокарда, то у меня есть основания включать измерение толщины стенки левого желудочка в исследование пациента с высоким ИМТ.
Лично я не в восторге от повсеместного использования словосочетания «комплексный подход», однако, если мы занимаемся ранней диагностикой и профилактикой, не думаю, что мы можем позволить себе роскошь исследования только одного органа или одной области.
Ожирение является предшественником воспаления. Уже идентифицировано множество молекулярных и генетических механизмов, которые объясняют, как запускается воспалительная реакция. Для наших целей нам следует рассматривать ожирение как хроническое воспаление, вызванное некой вялотекущей персистирующей инфекцией. Я не знаю, жир накапливающийся в клетках, повышает экспрессию или активирует провоспалительные гены, или же изменения являются результатом разрыва клеток, который ведет к воспалительной клеточной реакции.
В конечном итоге большое количество жира в печени приводит к воспалению. В самой печени выделяющие коллаген звездчатые клетки активируются воспалением. Хронический очаговый холецистит — это патофизиологическое воздействие на непосредственно прилегающий орган. Это важное связующее звено между многолетним ожирением и последующей желчнокаменной болезнью.
В последние несколько лет в сфере коммерческого ультразвука наблюдается повышенный интерес к диагностике фиброза печени, возможно вследствие осознания широкого распространения гепатита С. Вокруг очень много очевидно здоровых людей с ожирением, вредные последствия которого можно со временем устранить, поэтому проблемы этого состояния многие считают менее насущными, чем вирусные заболевания.
Каково бы ни было эмоциональное отношение к чрезмерному употреблению углеводов и алкоголя и боязни вирусного гепатита, фиброз представляет собой клинически важную проблему, ведь он способен влиять не только на качество, но и на продолжительность жизни. Наша задача — идентифицировать наличие потенциального риска (например, стеатоз) и определить наличие и степень фиброза.
Одной из основополагающих работ в сфере диагностического ультразвука, я всегда считал работу Fields S, Dunn F. Correlation of echographic visualizability of tissue with biological composition and physiological state. J Acoust Soc Am. 1973;54(3):809-12. То, что мы картируем с помощью ультразвука, это в основном модуль объемной деформации объемных элементов нашей выборки, в основном количество, тип и макроструктура коллагенового эндоскелета «мягких тканей».
Из-за множества крошечных участков коллагена паренхима печени выглядит грубой и гетерогенной и затухание ультразвука существенно увеличивается. Мне нравится получать увеличенные изображения небольших участков паренхимы печени, обычно с частотой от 5 до 7 МГц или от 15 до 18 МГц, где это возможно. О фиброзе обычно свидетельствуют яркие крапинки в секторе сканирования.
Если вдуматься, эластография — это способ увеличения контрастности тканей за счет снижения пространственного разрешения, и существует составной показатель (т.е. жесткость), который характеризует среднее значение этой характеристики. Это хорошо применимо к большим однородным измененным участкам. Здесь меня смущает то, что на мы хотим идентифицировать фиброз как при биопсии на микроскопическом уровне.
Я подозреваю, что имеет место небольшая вариабельность в оценке степени фиброза с помощью эластографии в зависимости от пульсации сосудов, фазы дыхания, контакта датчика с кожей. Независимо от того, используем мы усиленный акустический импульс или эластографию сдвиговой волны, двухмерная визуализация и эластография зависят от распространения ультразвуковой волны. Есть ли способ сделать эту общую информацию более видимой на традиционных изображениях?
Есть простое, но элегантное решение. Можно использовать любую имеющуюся в наличии ультразвуковую систему, дополнительных расходов нет.
Оценка жировой инфильтрации и/или фиброза печени включает оценку текстуры ткани. Это подобно тому, как мы видим различия между плетеной тканью и поверхностью полированного мрамора. Существуют способы числовой характеризации текстур, но они довольно сложные. Однако наши глаза и мозг быстро и хорошо справляются с такими задачами двумерного статистического распределения второго и третьего порядка.
Большую часть времени существования диагностического ультразвука было невозможно получить доступ к «сырым» данным принятого УЗ сигнала, на основе которых формируется отображаемое на мониторе изображение. Динамический диапазон этого набора данных намного шире диапазона, который могут отображать мониторы, поэтому сигнал преобразуется (логарифмическое сжатие) перед отображением на дисплее (ранее ТВ монитор).
Одно из преимуществ современных цифровые УЗ аппаратов - возможность экспортировать изображения, полученные до или во время отображения на мониторе. На некоторых устройствах это точечный рисунок BMP (это лучше всего), на других — сжатый JPEG (не лучший, но приемлемый вариант).
Это означает, что можно перенести изображения на флешку и потом открыть их на любом компьютере. То, с чем вы будете работать, довольно похоже на «сырые» УЗ данные, характеристики которых различимы при визуализации на обычном дисплее.
Далее необходимо загрузить одну из самых лучших программ обработки изображений ImageJ (J означает Java-программирование), она предоставляется бесплатно Американскими национальными институтами здоровья (NIH). Я обожаю эту программу. Последняя версия 1.48 обладает множеством функций и работает практически без задержек.
Я переношу УЗ изображения печени на компьютер и открываю их по одному в ImageJ. Выбираю область интереса. Я часто меняю яркость и контраст или степень дискретизации серой шкалы перед тем, как посмотреть на рисунок текстуры.
Это простой способ увеличения контраста и уменьшения шума серошкального изображения. Истинная ценность такой подготовки изображений в использовании дополнительных полуколичественных функций.
Одна из самых полезных, на мой взгляд, форм отображения для направляющих врачей — это трехмерное изображение, где сила сигнала представлена как высота. Жировая дистрофия печени представляет собой гладкие прерии, а фиброз выглядят как горная местность. Я также представляю распределение серой шкалы в виде гистограммы и использую двумерное преобразование Фурье для визуального отображения или расчета пространственного распределения групп отражающиъ ультразвук структур. Жаль, что размер этой статьи не позволяет мне рассказать об этом более подробно.
Ниже изображения еще одного пациента.
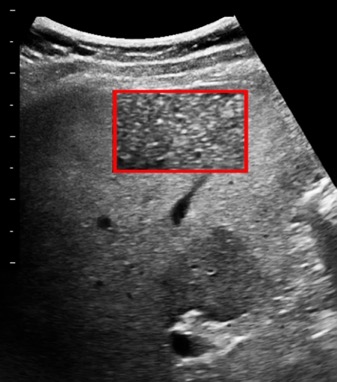
Изображение печени, область интереса 78 x 114 пикселей, полученное с помощью широкополосного датчика на опорной частоте 6МГц
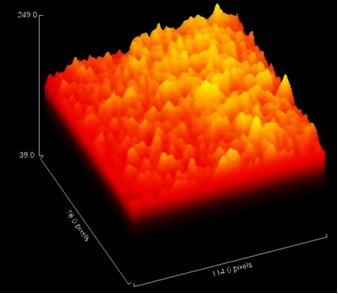
Пиковая амплитуда в области интереса, представленная по оси Z
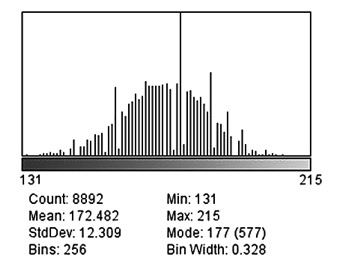
Гистограмма распределения уровней серой шкалы в области интереса
Что скажете по этому случаю? В моем отчете значилась жировая дистрофия печени (с включением нормальной области без жировых изменений) с начинающимся фиброзом. Это было подтверждено гистологически.
Я провел небольшое исследование на основе 50 пациентов, по которым смог получить дополнительную клиническую и лабораторную информацию.Печени отлично делились на нормальные, с жировой инфильтрацией и фиброзом только по одним лишь визуальным критериям. Стандартное отклонение на гистограмме серой шкалы стало самым лучшим самостоятельным числовым дифференцирующим и классифицирующим признаком. Ультразвуковая эластография не была полезной. Справедливости ради стоит отметить, что я смотрел здоровых амбулаторных пациентов, изображения которых очень сильно отличались от изображений госпитализированных пациентов с установленным и прогрессирующим заболеванием печени.
Я думаю, что на каком-то этапе производители начнут искать способы извлечения количественной информации из исходных «сырых» данных, полученных на традиционных сканерах. А пока существует простой способ улучшить восприятие серошкальных особенностей УЗ изображений.
Я знаю, что, используя какие-либо методы или технические хитрости, направленные на повышение качества изображений и извлечение из них максимальной пользы, вы лишь повысите свой уровень как специалиста ультразвуковой диагностики. Это касается любой области применения. Попробуйте ImageJ на изображении области интереса на плаценте по передней стенке, полученном с помощью датчика 15 или 18 MГц, и вы будете использовать этот прием во всех последующих исследованиях третьего триместра.
* Жировой гепатоз печени. Синонимы – стеатоз, жировая дистрофия печени, «жировая болезнь печени», стеатогепатоз ** Точка зрени автора *** Спекл **** Спасибо всем читателям, которые смогли дочитать публикациюКомментариев еще нет
Sirota Tamara Serfheevna
Мукажанова Асель Жаныбековна
Матишев Андрей Алексеевич
Погоцкая Наталья Станиславовна
Малтызова Разита Петровна
Малов Александр Константинович
Закиев Талгат Рифхатович
Шишова Ирина Анатольевна
Изранов Владимир Александрович